重要な理由は、その構造解析が
ガン治療や、寿命に関わることだからなのです。
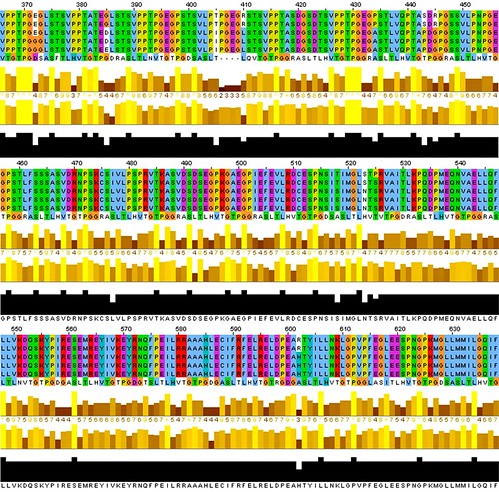
Nature 496, 7444
http://www.natureasia.com/ja-jp/nature/highlights/42957
記事閲覧に無料登録が必要な場合があります。
2013年4月11日
真核生物の線状の染色体の両端は、テロメラーゼと呼ばれるリボ核タンパク質複合体の働きによって維持されている。J Feigonたちは、ずっと以前から解明が待たれていた繊毛虫テトラヒメナ(Tetrahymena thermophila)のテロメラーゼの構造を、電子顕微鏡法によって決定した。さまざまな成分の結晶構造のモデル化によって、その触媒コアが明らかになり、サブユニット間の相互作用が解明された。また、この酵素のin vitroでの完全な再構築も行われた。その構造から、リボ核タンパク質触媒コア構造の詳細が新たに解明され、テロメラーゼとテロメアを結びつけ、テロメラーゼの連続反応性の基盤となるホロ酵素サブユニットの配置が明らかになった。
テロメアーゼが、なぜガン治療に役立ちそうなのか説明しているのがこちら。
結論だけになっているんですが、テロメアーゼは細胞分裂の最終的な回数を増やす機能があるのです。
生殖細胞や、ガン細胞では、この酵素が働いていて、いくらでも(もしくは相当回数)細胞分裂ができる、ということなんですね。
加齢遺伝学>老化の遺伝学(4)
4.テロメラーゼ
http://sugp.wakasato.jp/Material/Medicine/cai/text/subject07/no5/html/section4.html生殖細胞は末端複製問題を回避して長いテロメア長を維持している。これは、生殖細胞にはテロメアDNA末端にあらたにテロメアDNAを合成付加する酵素テロメラーゼ(telomerase)が高い活性を持って存在するためである。テロメラーゼはテロメア繰り返し配列という合成すべき配列を指定する鋳型RNAと複数の蛋白質とからなる複合体である。DNA複製の際にテロメア配列を5’から3’方向に合成伸長していくことにより、テロメア配列の短縮化を回避している。テロメラーゼは分化した正常体細胞では発現されていない。しかしながら、生殖細胞にくわえて、幹細胞(例:造血幹細胞)と多くの癌細胞では発現している。これらの細胞に共通する特徴は、無限の増殖能をもつことである。
その、テロメアーゼの研究成果を、ガン治療にどのように役立てようとしているのかが、こちら。
テロメア・テロメラーゼを分子標的としたがん治療
がん化学療法センター
http://www.jfcr.or.jp/chemotherapy/department/molecular_biotherapy/research/001a.html
私たちは、テロメア維持機構を標的とした新たながん治療法を確立することを目指し、基礎と応用の両視点から研究を進めています。とくに、新しいテロメラーゼ阻害剤を創製するとともに、培養がん細胞や実験動物レベルでその有効性を実証するなどの成果を上げてきました。現在はこれらの知見をもとに、新規阻害剤の探索・創製を継続するとともに、より実践的な治療モデルの構築、テロメア動態制御ネットワークの描出と薬剤感受性の相関解析、テロメラーゼの新機能の解析などを行っています。
2.テロメラーゼ阻害剤の耐性および効果増強
がん細胞のテロメアは、テロメラーゼによって無制限に伸長しているわけではなく、正常細胞よりもむしろ短い場合が多いことが報告されています。テロメアにはシェルタリン(shelterin)と呼ばれる蛋白質複合体が結合しており、これがテロメラーゼのテロメアへのアクセスを制限しているのです。長いテロメアほどより多くのシェルタリンが結合しますので、テロメラーゼが負のフィードバックを受けてテロメア伸長反応が起こりにくくなります。逆に、短いテロメアではシェルタリンが少なくなり、テロメラーゼが働きやすくなります。私たちは、テロメラーゼ阻害剤によるテロメアの短縮が、染色体末端のシェルタリン存在量を減らし、僅かに残存するテロメラーゼ活性のテロメアへのアクセスを増強してしまうということを見出しました(Cancer Cell 2005)。テロメラーゼ阻害剤によるテロメア短縮が、テロメラーゼ阻害剤耐性を引き起こす、というパラドックスです。
見方を変えれば、テロメラーゼ阻害剤の制がん効果は、テロメア短縮の効率化をはかることで改良されると期待されます。シェルタリンの構成因子のなかでも特に、TRF1と呼ばれる蛋白質のテロメア結合が、テロメラーゼのテロメアへのアクセスを遮断するカギ分子となります。私たちは、TRF1がタンキラーゼ1(tankyrase-1)と呼ばれるポリ(ADP-リボシル)化酵素(PARP)の働きによってテロメアから遊離することに着目しました。そして、タンキラーゼ1によるテロメアからのTRF1の遊離が、テロメラーゼのテロメア会合を促進し、テロメラーゼ阻害剤耐性を誘導することを見出しました。さらにこれとは逆に、タンキラーゼ1の働きを止めるPARP阻害剤が、テロメラーゼ阻害剤のテロメア短縮効果を増強し、標的がん細胞の死期を早めることを明らかにしました(Cancer Cell 2005, Br J Cancer 2006)。
正常細胞内でも機能する酵素ですから、当然副作用もある薬剤です。
更なる研究と、効果的な治療法の発展につながればよいですね!